在制药行业的数字化领域,有一个现象正变得越来越突出:头部药企花费两三年时间、投入数百万元才完成验证的合规系统,到了中小药企这里,往往还要重新走一遍同样的路。
这背后所反映出的,是制药行业数字化进程中一个长期被忽略的“经验断层”问题。科伦药业在搭建覆盖生产、质量、研发等全流程的电子记录系统时所遇到的各种难题,绍兴民生医药在构建QMS质量管理体系过程中所经历的种种摸索——这些被头部企业用大量资金和时间换来的验证成果,本可以成为整个制药行业的公共财富,却在传统的软件交付模式下,被牢牢地锁在了每一家企业自己的围墙之内。
问题的根本在于交付逻辑。传统模式下,软件厂商交付给客户的是一套“代码”,而不是一个“平台”——每一家企业的系统都是独立开发的实例,验证成果无法跨企业复用,行业经验也难以有效沉淀。而魔方网表作为可配置数字化平台,其独特之处在于采用了“平台+模板”的分层架构,将头部企业已经验证过的合规能力提炼成标准化的组件,使得中小药企可以直接继承这些成果,真正实现GMP合规“不再从零开始”。
合规底座:经过头部企业验证的“地基工程”
要理解为什么魔方网表能够让中小药企直接继承头部企业的验证成果,首先需要弄清楚它在GAMP5体系中所处的位置。
魔方网表属于GAMP5标准定义下的第4类软件——即可配置软件,它介于第3类“不可配置的标准软件”与第5类“定制开发软件”之间。这一分类赋予了它一个非常关键的属性:平台本身已经将GMP、GLP、GCP等各类医药行业规范要求内化成了底层的组件和基础特性,凡是使用魔方网表搭建出来的系统,天然就符合医药行业的合规要求,企业只需要完成自我验证即可满足CSV规范。
换句话说,魔方网表的合规能力不是靠后期“打补丁”添加上去的,而是从架构设计的最底层就被“内嵌”到了平台之中。这意味着,每一次功能配置和后续调整,都会自动遵循合规逻辑,企业完全不必为了每一次系统升级而重复投入大量的验证资源。
更值得强调的是,这种合规能力已经经过了头部企业的实战检验。科伦药业选择将魔方网表作为其数字化转型的基座,构建了一个全面覆盖生产、质量、研发等关键业务环节的电子记录系统。魔方网表的技术团队与科伦药业紧密配合,深入研究了各项业务需求,快速搭建起系统架构,并经过多轮迭代测试,确保了系统的稳定与可靠。通过这套系统,科伦药业实现了关键数据的自动采集与录入,大幅减少了人工输入带来的差错;实现了对生产过程的实时监控,确保了各项操作的规范性;同时,魔方网表强大的追溯功能,也让管理人员可以快速定位并查看任意数据的历史记录,从而充分满足监管方面的要求。
绍兴民生医药则利用魔方网表,打造了一套既符合GMP规范、又支持灵活配置的QMS质量管理系统。该系统帮助民生药业建立了标准化的质检流程,通过自动化的流程流转,实现了对不同流程节点的任务分配与执行情况的精细管控。系统自带的实时数据跟踪与监控功能,使得质量管理模式从传统的“事后检查”逐步转向了“过程管控”。
这些头部企业“踩过的坑、填过的土”,最终都沉淀在了魔方网表平台的底层能力以及标准化的模板之中。对于中小药企而言,他们不再需要从零开始搭建合规架构——平台的底层组件和标准化模板已经承载了头部企业的验证成果,他们只需数周时间,就能完成系统部署并正式上线运行。
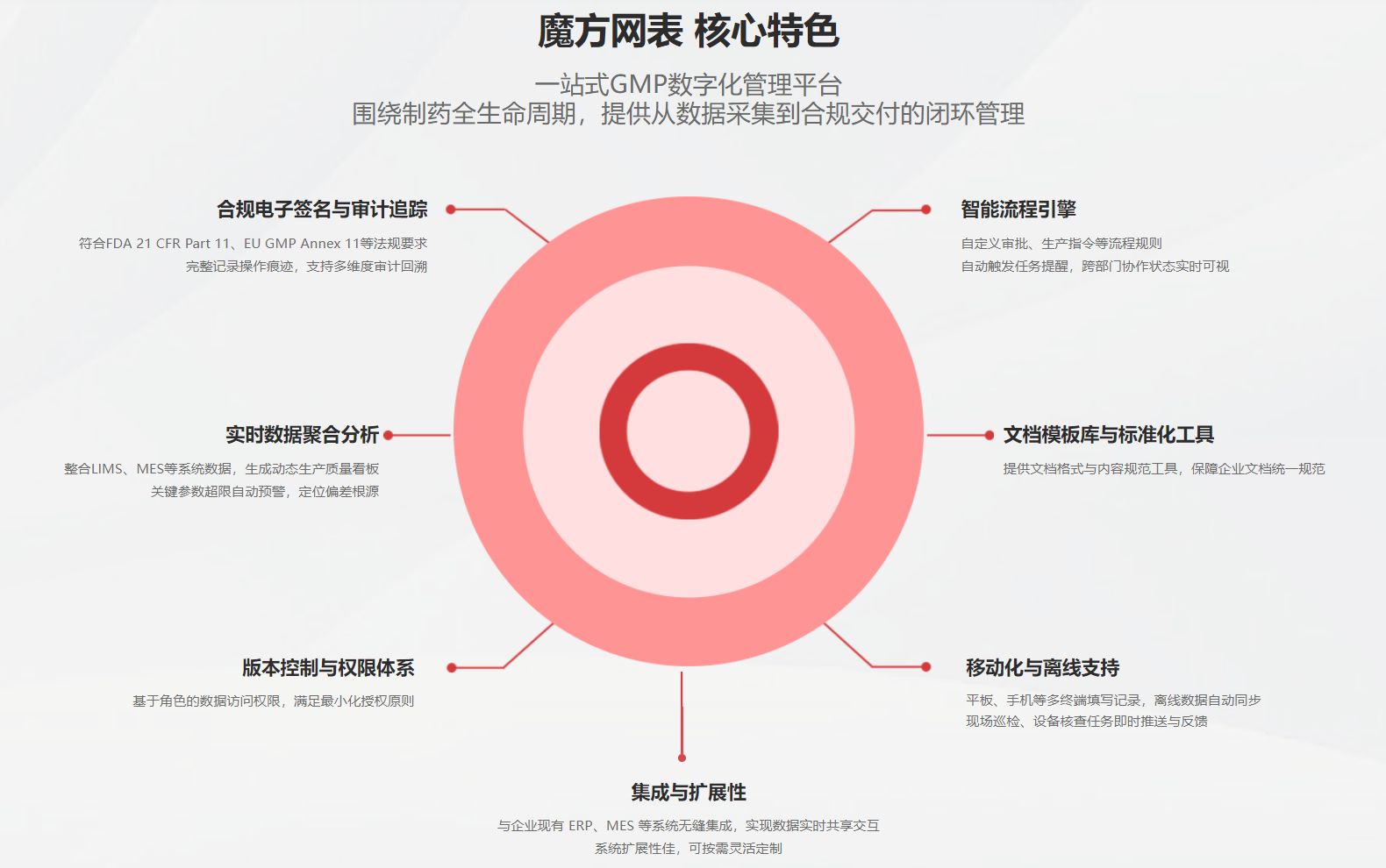
质量三件套:让行业经验变得可复制
如果说平台底层能力是合规的“地基”,那么基于平台预先配置的行业模板,就是将头部企业的业务经验转化为可复用的“标准化产品”的关键一环。
魔方网表针对制药行业最核心的质量管理需求,预先配置了“药企质量管理三件套”——也就是QMS(质量管理系统)、DMS(文档管理系统)和TMS(培训管理系统)三套标准化模板。这些模板并不是僵化不变的“黑盒”软件,而更像是一套经过精心设计的“乐高积木”——平台已经搭建好了质量管理体系的基本框架和行业最佳实践,确保了下限也就是合规底线,同时企业完全可以依据自身的SOP、组织架构和业务流程,灵活调整页面的布局、审批的流程、字段的设置以及报表的格式。
这正是中小药企最需要的能力。头部企业有能力投入大量资源,定制一套与自身流程完全匹配的系统,但中小药企通常没有这样的预算和人力。然而,有了“三件套”模板之后,中小药企不再需要“从零设计”,而是可以在已经被行业验证过的最佳实践基础上,按需进行适配和调整——他们继承的是头部企业沉淀下来的流程智慧,需要做的只是针对自身特性进行微调。
以DMS为例,魔方网表的DMS覆盖了文件从起草、评审、批准、发布、生效、分发、复审,到作废与归档的全流程管理。它将合规控制——包括电子签名、审计追踪、版本管理、权限控制——作为系统的默认能力,大幅降低了人工合规的工作负担。这意味着中小药企不必再自己去设计文件管理流程,也不必担心流程中可能出现哪些合规盲区——头部企业已经验证过的流程逻辑,直接就可以“开箱即用”。
同样,魔方网表还将审计追踪、电子签名、二次认证这三大合规核心功能进行了整合,实现了“一站式启用”。当用户执行某项业务操作时,系统会同步触发相关的合规流程:操作过程自动被纳入审计追踪范围,操作完成后若需要确认则会启动电子签名流程,而如果涉及高风险环节,系统还会自动触发二次认证。整个过程形成了一个“操作-记录-确认-追溯”的完整合规闭环。这种将三大功能深度融合的设计,无需药企额外开发或整合多套系统,就能让合规管理与业务流程融为一体,极大地降低了中小药企在合规实施方面的门槛。

从“单打独斗”到“平台赋能”:中小药企的合规新路径
在传统模式下,中小药企推进GMP合规数字化的路径大致是这样的:立项→选型→需求分析→开发或采购→CSV验证→上线。每一个环节都是相对孤立的项目行为,每一家企业都在重复造轮子。更棘手的是,由于中小药企预算普遍有限,往往只能选择功能相对固化的标准软件,最终常常陷入“买了系统却用不起来”的尴尬局面。
魔方网表所代表的模式则完全不同。平台的底层合规能力已经经过了头部企业的验证,“三件套”模板承载了行业内的最佳实践,外部字段组技术可以轻松对接企业现有的ERP、LIMS、MES等各类系统,有效避免数据孤岛的出现。中小药企需要做的事情被大幅简化:在平台和模板的基础上,快速配置出符合自身需求的应用,自主完成CSV验证(也可以借助魔方网表提供的CSV验证支持服务),系统上线之后还可以根据业务变化随时灵活调整。
这种模式的价值,绝不仅仅是省钱和省时间,更在于它将中小药企从“合规项目的实施者”转变成了“合规能力的运营者”。企业不再需要花费大量精力去研究“到底什么样的系统才算合规”,而是可以直接在一个已经被验证为合规的平台上,集中精力去思考如何用系统解决自己的实际业务问题。
制药行业的GMP合规数字化,发展到今天,已经不应该再是“每一家都要从头干一遍”的阶段了。科伦药业走过的路,民生医药趟过的河——这些头部企业用真金白银换来的验证成果,理应成为整个行业可以共享的基础设施。
魔方网表作为可配置数字化平台的价值,正在于此。它以“平台+模板”的模式,将头部企业的验证成果沉淀为可复用的能力组件,让中小药企能够站在巨人的肩膀上,把有限的精力和资源聚焦到业务创新上,而不是重复进行低效的验证工作。当合规底座不再是需要每一家企业自行建造的“地基工程”,而是可以直接继承的“行业基础设施”时,中小药企的GMP合规才能真正从“及格线边缘的挣扎”走向“真正的质量竞争力”。
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。